近日,我校重质油国家重点实验室新型碳材料团队的徐文刚副教授关于含氟有机分子的工作被化学领域顶级期刊《德国应化》接收。同时,徐文刚副教授获批中国博士后基金国际交流引进项目,获得40万元的资助。
约20%的药物及30%的农药分子中含有碳氟键,而含氟有机分子无法自然合成。所以利用含氟构筑单元合成有机氟化物的研究,日益受到关注。该类化合物在药物、杀虫剂、催化剂和材料等领域有广泛应用。尽管选择性氟化已经取得了极大的进展,但是选择性的合成多氟有机化合物仍然极具挑战。本文中,氟代有机硼烷可以作为构筑多氟有机物的结构单元。该类化合物可以通过多氟化合物的选择性脱氟硼烷基化合成,即多氟有机化合物的选择性C–F键硼化。然而,这一课题本身就具有挑战性,原因如下:1)C–F键是最惰性的官能团之一;2)金属氟键的高键能会导致过渡金属催化C–F活化效率极低;3)硼试剂一般是高度亲氟的,通常作为氟原子捕获剂。
多氟芳烃和烯烃通过光催化C–F键功能化构筑C–C键已有报道。多氟芳烃和偕二氟烯烃可在光催化条件下,实现单电子还原,之后氟负离子离去,产生多氟芳基自由基从而参与到一系列碳碳键的形成反应中。另外,光催化N-杂环卡宾硼烷的氢转移反应可以得到硼自由基。综上,本文提出通过光催化和氢转移催化协同作用,实现N-杂环卡宾硼烷的直接B–H活化,最终实现多氟有机物脱氟硼烷基化。

该工作利用原子经济性更好的氮杂环卡宾硼烷代替联硼酸频那醇酯作为硼化试剂,在可见光诱导下实现多类有机氟化物的脱氟硼化反应。反应的适用范围广。尤其对多氟代芳烃,反应的区域选择性极高。通过对反应中间体的电荷密度进行理论计算,发现碳氟键的断裂发生在更负电性位置。同时,对含氨基的底物,反应的选择性还受分子内氢键影响。反应中C–F键断裂的选择性与过渡金属催化有明显不同。该反应条件温和,相较于过渡金属催化的反应,官能团耐受性更好。
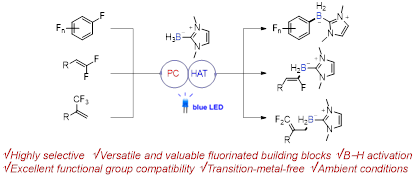
作者通过光氧化还原和氢转移催化诱导的B–H键活化,以原子和氧化还原经济的方式开发了一种实用的多氟芳烃、偕二氟烯烃和三氟甲基烯烃的脱氟硼烷基化反应。反应选择性很高,可以与过渡金属催化的脱氟硼化反应相互补充。具有不同氟代程度和多功能化的氟代有机硼烷可通过简单操作,在温和的条件,甚至是无过渡金属催化条件下获得。反应产物作为多氟代有机物的构筑单元可能在含氟药物、催化剂、材料的合成方面得到广泛应用。然而,该反应中多氟代芳烃碳氟键切断的选择性仍然没有很好地解释,这将是我们未来需要解决的重要问题。
该研究成果“Visible-Light-Induced Selective Defluoroborylation of Polyfluoroarenes, gem-Difluoroalkenes, and Trifluoromethylalkenes”的第一作者为徐文刚博士,中国石油大学(华东)新能源学院特任副教授。2019年09月加入新型碳材料研究室吴明铂团队。主要从事光化学合成,电化学合成及小分子活化等领域的研究工作。通讯单位为新加坡国立大学化学系,中国石油大学(华东)新能源学院及重质油国家重点实验室等。
文章附件: DOWNLOAD.pdf
DOWNLOAD.pdf

